目前,國內外已經(jīng)批準6款CAR-T療法,詳見(jiàn)下表。除了Abecma,另外5款均靶向CD19。
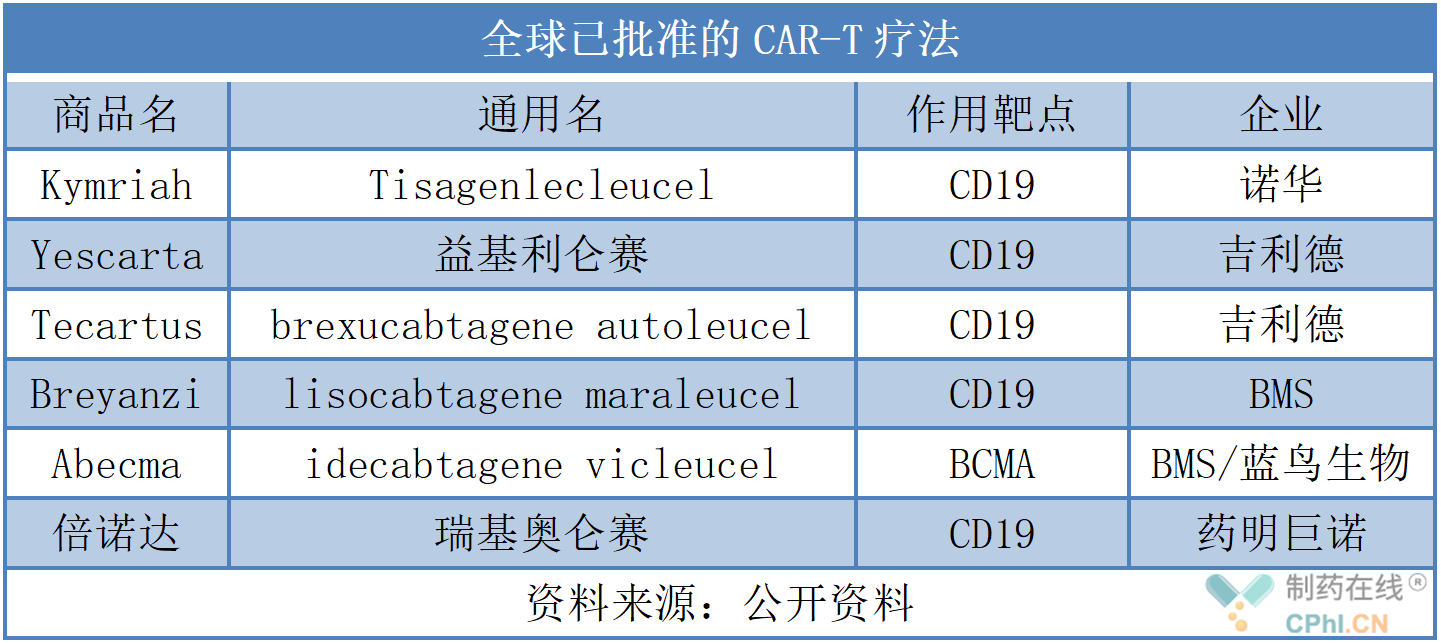
隨著(zhù)公司財報的公布,2021年上述5款CAR-T療法的銷(xiāo)售額也順勢出爐,其中瑞基奧侖賽是藥明巨諾在美國 Juno 公司 JCAR017 (即Breyanzi)基礎上開(kāi)發(fā)的一款CAR-T療法,2021年9月在國內被NMPA批準用于治療經(jīng)過(guò)二線(xiàn)或以上全身性治療后成人患者的復發(fā)或難治性大B細胞淋巴瘤。
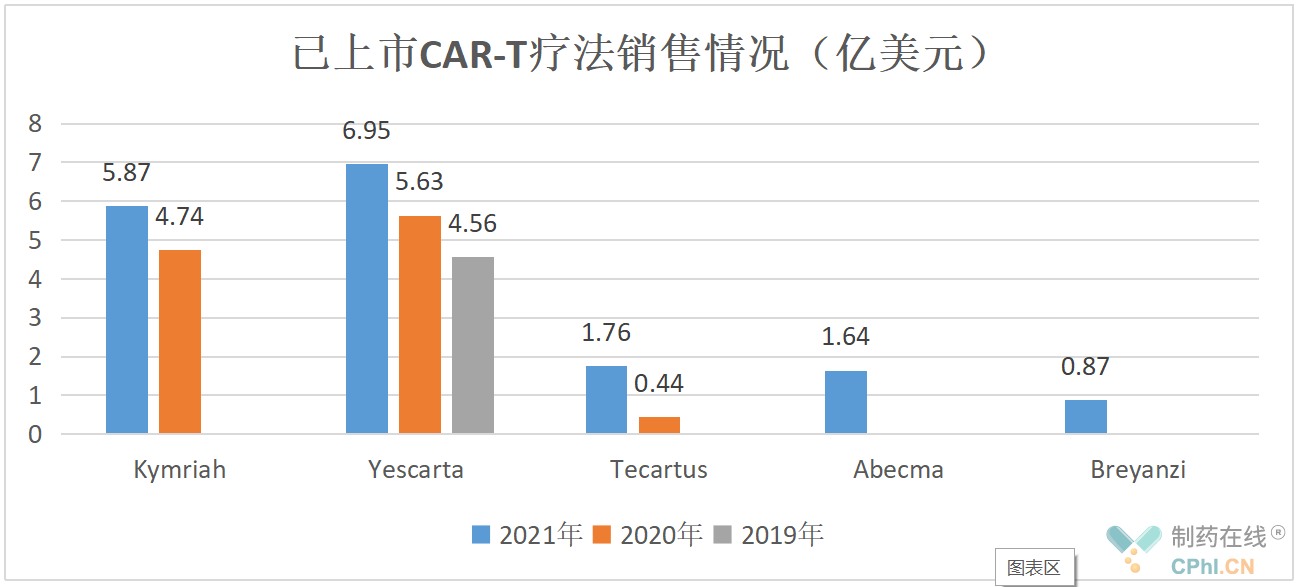
從時(shí)間軸上看,2019年至2021年CAR-T療法市場(chǎng)規模不斷擴大,這三年CAR-T療法的市場(chǎng)規模分別為7.34億美元、10.81億美元和17.09億美元。而據弗若斯特沙利文報告:2019年至2024年CAR-T療法市場(chǎng)規模復合年增長(cháng)率為55.0%,2024年將增長(cháng)至66億美元;2024年至2030年復合年增長(cháng)率預計為22.1%,2030年將進(jìn)一步增長(cháng)至218億美元。由此可見(jiàn),目前CAR-T市場(chǎng)遠未飽和,亟待企業(yè)挖掘。
回顧2021,多款CAR-T療法在監管方面取得新進(jìn)展:
Breyanzi
2021年2月被FDA批準用于治療先前已接受過(guò)2種或2種以上系統療法的復發(fā)或難治性大B細胞淋巴瘤(R/R LBCL)成人患者;
2021年3月在日本被批準用于治療復發(fā)或難治性大B細胞淋巴瘤(R/R LBCL),以及復發(fā)或難治性濾泡性淋巴瘤(R/R FL);
Abecma
2021年3月被FDA批準用于治療既往接受過(guò)4種或更多種療法(包括免疫調節劑、蛋白酶體抑制劑、抗CD38抗體)的復發(fā)性/難治性多發(fā)性骨髓瘤(R/R MM)成人患者;
2021年8月獲EC附條件批準用于治療先前已接受過(guò)至少3種療法治療(包括免疫調節劑、一種蛋白酶體抑制劑、一種抗CD38抗體)且在最后一種療法治療期間疾病進(jìn)展的R/R MM成人患者;
Tecartus
2021年10月被FDA批準用于治療復發(fā)或難治性B細胞前體急性淋巴細胞白血病(ALL)成人患者
Yescarta
2021年1月在日本被批準用于治療某些復發(fā)/難治性大B細胞淋巴瘤(LBCL)成人患者
2021年3月被FDA批準用于治療先前已接受過(guò)2種或多種系統療法的復發(fā)性或難治性(R/R)濾泡性淋巴瘤(FL)成人患者
2021年10月向FDA遞交二線(xiàn)治療復發(fā)或難治性大B細胞淋巴瘤(LBCL)成人患者的sBLA
Kymriah
2021年10月FDA和EMA受理其用于治療先前接受過(guò)至少2種療法的復發(fā)或難治性濾泡性淋巴瘤(r/r FL)成人患者的新適應癥上市申請;
此外,2021年楊森和傳奇生物聯(lián)合開(kāi)發(fā)的BCMA靶向的CAR-T療法Carvykti(cilta-cel)向FDA遞交了治療復發(fā)/難治性多發(fā)性骨髓瘤(MM)成人患者的BLA。相信隨著(zhù)新適應癥和新產(chǎn)品的獲批,未來(lái)CAR-T療法市場(chǎng)將進(jìn)一步擴大。
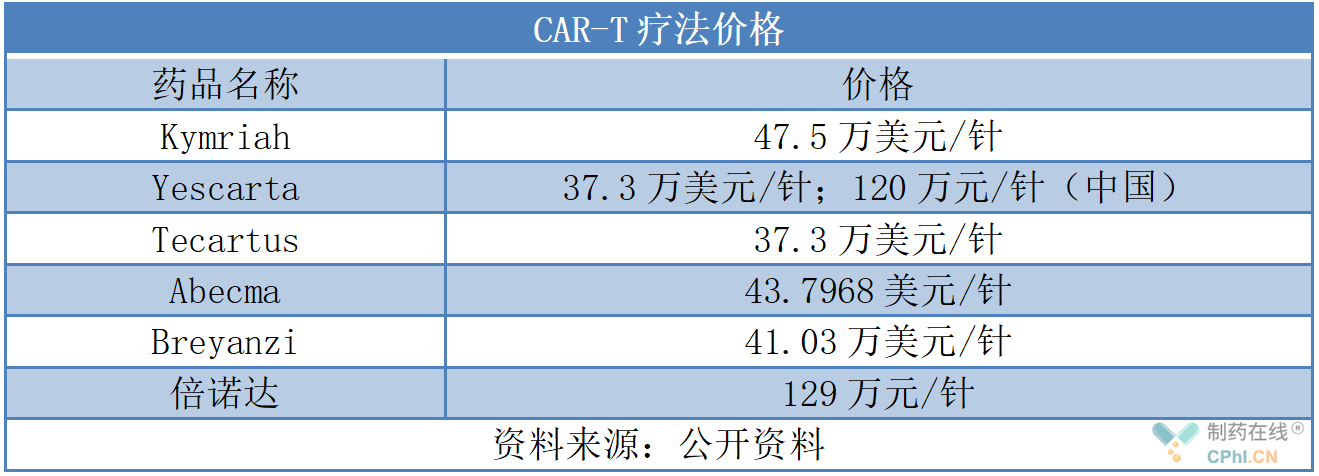
不過(guò),CAR-T療法要想惠及更多患者必須解決價(jià)格問(wèn)題。目前,CAR-T價(jià)格可謂天價(jià),最 便宜的也在100萬(wàn)元以上。



合作咨詢(xún)
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博華國際展覽有限公司版權所有(保留一切權利)
滬ICP備05034851號-57
2006-2025 上海博華國際展覽有限公司版權所有(保留一切權利)
滬ICP備05034851號-57