好日子誰(shuí)都想過(guò),但復宏漢霖偏不。
2022年,僅漢利康、漢曲優(yōu)和漢達遠3款產(chǎn)品,就為復宏漢霖帶來(lái)23.58億元收入(含授權許可收入),然而為了長(cháng)久的“幸福”,復宏漢霖將錢(qián)砸向研發(fā),毅然選擇繼續勒緊褲腰帶“吃苦”,終于在2023年迎來(lái)了曙光。
近日,復宏漢霖發(fā)布了2023年正面盈利預告,全年利潤不低于5億元,值得一提的是,這是復宏漢霖首次實(shí)現年度盈利。
從虧損到盈利,復宏漢霖靠什么華麗轉身?
01
做仿制,
實(shí)現Biopharma的早期出彩
復宏漢霖的5款上市產(chǎn)品,分別為利妥昔單抗(漢利康)、曲妥珠單抗(漢曲優(yōu))、阿達木單抗(漢達遠)、貝伐珠單抗(漢貝 泰)和斯魯利單抗(漢斯狀),前4款均為生物類(lèi)似藥。
精準定位,仿制同樣也能差異化。復宏漢霖的漢利康是其首 款獲批上市的產(chǎn)品,也是國內首 個(gè)獲批的利妥昔單抗生物類(lèi)似藥,率先打破了進(jìn)口藥壟斷格局。
然而,僅打破進(jìn)口壟斷還不僅僅是復宏漢霖的目標,因原研藥在國內未獲批類(lèi)風(fēng)濕關(guān)節炎適應癥,復宏漢霖瞄準適應癥差異化“缺口”,在2022年3月獲批了該適應癥,讓漢利康在適應癥覆蓋面上趕超原研藥,大大增加了撕開(kāi)被壟斷市場(chǎng)的成功幾率,據藥智數據顯示,漢利康自上市以來(lái),年度銷(xiāo)售額持續增長(cháng),2022年為17.13億元,同比增長(cháng)18.04%。
適應癥的差異化布局,讓漢利康在海外同樣“受寵”,2023年4月,Boston Oncology與復宏漢霖達成合作協(xié)議,獲得在沙特阿拉伯、埃及、巴林等中東和北非地區商業(yè)化漢利康的權利,但這不并不是復宏漢霖的生物類(lèi)似藥首次“走出”國門(mén)。
瞅準市場(chǎng),與原研藥PK國際市場(chǎng)。漢曲優(yōu)是復宏漢霖獲批上市的第2款產(chǎn)品,為曲妥珠單抗(赫賽汀)生物類(lèi)似藥,由于赫賽汀在全球范圍均屬昂貴藥物,2018年時(shí),單瓶(440毫克)在美國的價(jià)格為4500-5100美元,在歐盟,則以單劑量(150毫克)銷(xiāo)售,價(jià)格為500-700美元,此外,盡管赫賽汀已被納入國家醫保目錄大幅降價(jià),但單瓶(440毫克)價(jià)格仍高達7270元,據弗若斯特沙利文報告顯示,當時(shí)中國僅有約25%患者能負擔治療費用。
復宏漢霖抓住市場(chǎng)機遇,及時(shí)布局,讓漢曲優(yōu)成為首 款在中國開(kāi)發(fā)且同時(shí)在全球多個(gè)地區進(jìn)行3期臨床試驗的赫賽汀生物類(lèi)似藥。2020年7月,漢曲優(yōu)在歐盟獲批上市,成為首 個(gè)在歐盟獲批的國產(chǎn)單抗生物類(lèi)似藥,2020年8月,漢曲優(yōu)又在國內獲批,又一次打破進(jìn)口藥的壟斷。
時(shí)至今日,漢曲優(yōu)已成為國產(chǎn)生物類(lèi)似藥“出海”代表,據復宏漢霖2023半年報顯示,已在約40個(gè)國家和地區獲批上市,上半年實(shí)現銷(xiāo)售收入12.39億元,同比增長(cháng)54.8%。
還有多款重磅仿制藥在手。據復宏漢霖2023半年報顯示,產(chǎn)品管線(xiàn)中已處于IND及以上階段的單抗類(lèi)似藥還有6款,分別為HLX11(帕妥珠單抗)、HLX14(地舒單抗)、HLX05(西妥昔單抗)、HLX15(達雷妥尤單抗)、HLX13(伊匹木單抗)和HLX17(帕博利珠單抗),其中,HLX11和HLX14已處于3期臨床階段。

圖1 復宏漢霖進(jìn)入臨床階段產(chǎn)品管線(xiàn)
圖片來(lái)源:復宏漢霖2023半年報
值得一提的是,HLX11和HLX14如漢曲優(yōu)一樣也采取國際化戰略開(kāi)發(fā),進(jìn)行了國際多中心臨床研究,其中,HLX11已獲中國和歐盟臨床許可,HLX14已獲中國、歐盟和澳大利亞臨床許可。
02
為創(chuàng )新,
不惜再苦熬幾年
4款生物類(lèi)似藥的陸續獲批上市,為復宏漢霖帶來(lái)了營(yíng)收的持續劇增,到2022年,僅漢利康、漢曲優(yōu)和漢達遠3款產(chǎn)品就為其帶來(lái)23.58億元的收入(含授權許可收入),然而,復宏漢霖仍無(wú)法實(shí)現盈利,原因在于研發(fā)上的巨額支出,2022年研發(fā)開(kāi)支為13.95億元,同比增長(cháng)36.19%,這也解釋了復宏漢霖賺的錢(qián)都去哪了。
一切為了創(chuàng )新。梳理復宏漢霖歷年研發(fā)開(kāi)支可以發(fā)現,其也算的上是研發(fā)上的“燒錢(qián)王”,產(chǎn)品一路獲批的越多,反而研發(fā)開(kāi)支卻越來(lái)越大,在第4款產(chǎn)品漢貝 泰獲批(2021年12月)后的2022年,研發(fā)開(kāi)支反而是首 款產(chǎn)品獲批(2019年2月)前一年度的近4倍,5年時(shí)間研發(fā)開(kāi)支總額超43億元。
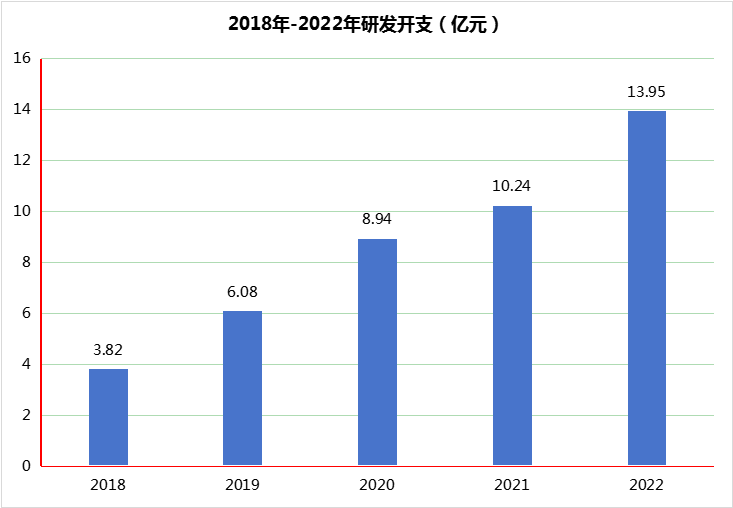
圖2 復宏漢霖2018年-2022年研發(fā)開(kāi)支情況
數據來(lái)源:復宏漢霖歷年年報
復宏漢霖本可憑借4款產(chǎn)品迎接利潤“黎明”,卻“為難”自己在虧損的“黑暗”中繼續前行數年。據其招股書(shū)顯示,在2019年時(shí),管線(xiàn)中就包含多款創(chuàng )新藥,其中,HLX06、HLX07、HLX10、HLX20和HLX22已經(jīng)進(jìn)入臨床階段。
先苦后甜,終于迎來(lái)“天”亮。2022年,復宏漢霖首 款自研創(chuàng )新藥斯魯利單抗(漢斯狀)獲國家藥監局批準上市,雖然漢斯狀為PD-1單抗,但卻是全球首 個(gè)獲批用于一線(xiàn)治療廣泛期小細胞肺癌(ES-SCLC)的PD-1藥物,再一次的差異化布局,讓這款PD-1的“后來(lái)者”在PD-1/L1極度內卷的市場(chǎng)中站穩腳跟。
據復宏漢霖2023半年報顯示,漢斯狀上半年實(shí)現銷(xiāo)售收入5.56億元,值得一提的是,2022年12月,復星醫藥獲得漢斯狀在美國商業(yè)化權利,復宏漢霖將獲得10億元首付款和不超7億元里程碑付款,截至2023年6月,已收到9億元許可費用。
此外,漢斯狀也得到國外藥企青睞,2023年8月,KGbio進(jìn)一步擴大與復宏漢霖在2019年關(guān)于漢斯狀的合作,進(jìn)而獲得沙特阿拉伯、埃及等12個(gè)國家包括ES-SCLC在內的2項適應癥獨家權利;2023年10月,Intas Pharmaceuticals與復宏漢霖達成合作,獲得歐洲地區和印度現有適應癥獨家權利。
筆者分析,復宏漢霖2023年的首次年度盈利,除了漢斯狀銷(xiāo)售收入持續增長(cháng)的獲益外,很大程度上得利于下半年幾筆漢斯狀海外授權的首 款款及里程碑付款收入。
值得一提的是,2023年12月,KGbio成功將漢斯狀在印度尼西亞獲批用于治療ES-SCLC,實(shí)現了漢斯狀海外市場(chǎng)進(jìn)軍的第一步。截至2023年底,漢斯狀用于ES-SCLC的歐盟上市申請已獲受理,同樣適應癥的美國橋接試驗也正在進(jìn)行中,此外,用于局限期小細胞肺癌的國際多中心試驗在美國、澳大利亞、歐盟已處于3期階段,漢斯狀海外進(jìn)軍路已越走越寬。
03
“天”亮后,
全面創(chuàng )新期開(kāi)啟
如今的復宏漢霖,臨床管線(xiàn)項目早已不再是生物類(lèi)似藥的天下,除了臨床前產(chǎn)品均為創(chuàng )新藥外,IND及以上階段的項目也以創(chuàng )新藥為主,且異常豐富,包括單抗創(chuàng )新藥HLX04-O、HLX07、HLX22、HLX60和HLX51;雙抗創(chuàng )新藥HLX301;融合蛋白創(chuàng )新HLX53;ADC藥物HLX42和HLX43;小分子創(chuàng )新藥HLX208,以及圍繞漢斯狀開(kāi)發(fā)的多個(gè)臨床項目。

圖3 復宏漢霖非生物類(lèi)似藥管線(xiàn)
圖片來(lái)源:復宏漢霖2023半年報
HLX04-O是復宏漢霖在上市產(chǎn)品貝伐珠單抗(漢貝 泰)基礎上進(jìn)行優(yōu)化,自主研發(fā)的重組抗VEGF人源化單克隆抗體眼科產(chǎn)品,截至2023年7月,用于濕性年齡相關(guān)性黃斑變性(wAMD)患者的國際多中心3期臨床研究,已在歐盟國家拉脫維亞、澳大利亞及美國完成首例患者給藥,據1/2期臨床研究結果顯示,HLX04-O在wAMD患者中安全性和耐受性良好,且展現出初步療效。
HLX07是復宏漢霖自主研發(fā)的靶向EGFR創(chuàng )新生物藥,截至2023年底,已在中國、美國、歐盟、澳大利亞、日本等多個(gè)國家地區獲得專(zhuān)利,且在中美獲得臨床試驗許可,值得一提的是,復宏漢霖還圍繞食管鱗癌、鱗狀非小細胞肺癌、皮膚鱗癌等多個(gè)實(shí)體瘤適應癥,開(kāi)展HLX07單藥或聯(lián)合的2期臨床探索。
據一項HLX07聯(lián)合漢斯狀與化療聯(lián)用一線(xiàn)治療晚期/復發(fā)性鱗狀非小細胞肺癌患者2期研究數據顯示,A組(6例)和B組(6例)根據RECIST 1.1評估未確認的ORR分別為83.3%和66.7%,兩組的疾病控制率均為100.0%,該研究結果在2023年歐洲腫瘤學(xué)會(huì )亞洲分會(huì )(ESMO Asia)年會(huì )上得以展示,一同展示的還有小分子創(chuàng )新藥HLX208。
2023年4月,HLX208被正式納入突破性治療品種名單,用于治療BRAF V600E突變的成人朗格漢斯細胞組織細胞增生癥(LCH)和Erdheim-Chester病(ECD),ECD與LCH均為《第一批罕見(jiàn)病目錄》中的疾病。
隨著(zhù)上述產(chǎn)品臨床試驗進(jìn)展的加持,復宏漢霖創(chuàng )新藥研發(fā)實(shí)力將全面崛起。
04
結語(yǔ)
好日子誰(shuí)都想過(guò),尤其是憑借已獲批產(chǎn)品實(shí)現營(yíng)收暴漲的復宏漢霖,過(guò)幾天好日子更是理所當然,但為了長(cháng)久“幸福”,毅然選擇繼續“吃苦”,終于在2023年迎來(lái)了光明,這段堅守初心靜待花開(kāi)的歷程值得同行參考學(xué)習。








合作咨詢(xún)
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博華國際展覽有限公司版權所有(保留一切權利)
滬ICP備05034851號-57
2006-2025 上海博華國際展覽有限公司版權所有(保留一切權利)
滬ICP備05034851號-57